
钠坐落元素周期表中第三周期ⅠA族,最外层只需1个电子,在化学反响中易失掉最外层电子而出现+1价,因此钠在化学反响中表现出较强的复原性。
钠的取用办法:用镊子夹取一小块钠,用滤纸吸干外表的火油,用小刀切取黄豆巨细的钠,剩下的钠放回原试剂瓶。
无论是CO2或H2O(g)的单一物质仍是二者的混合物,与足量的Na2O2反响时,耗费CO2或H2O(g)与放出O2的物质的量之比均为2∶1,即气体减小的体积等于生成的O2的体积。

定论:凡分子组成契合(CO)m(H2)n的物质,m g该物质在O2中彻底焚烧,将其产品(CO2和水蒸气)经过足量Na2O2后,固体增重必为mg。或者是由C、H、O三种元素组成的物质,只需C、O原子个数比为1∶1,即可满意上述条件。

定论:若CO2和水蒸气的混合气体(或单一气体)经过足量的Na2O2,则气体体积削减的量等于原混合气体体积的,且等于生成氧气的体积。
一定量Na2O2与一定量CO2和H2O(g)的混合物反响,处理问题时可视作Na2O2先与CO2反响,待CO2反响完成后,Na2O2再与H2O(g)产生反响(实践情况复杂得多)。
不论是与CO2仍是与H2O(g)反响,CO2与H2O(g)均既不是氧化剂也不是复原剂,反响的本质都是Na2O2本身产生的氧化复原反响,所以每有1 mol O2生成时,搬运的电子均为2 mol。
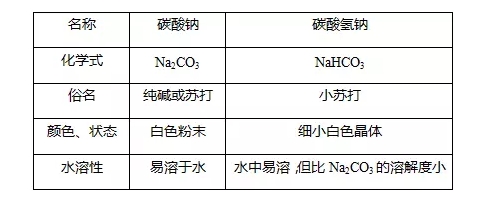
补白:因NaHCO3的溶解度较小,将CO2通入到饱满Na2CO3溶液时,开端无明显现象,后有沉积分出。
扫描免费领近十年高考真题汇总备考、选科和专业解读重视高考网官方服务号
搪瓷反应釜厂家华体会导航官方首页-hth体育,主要生产销售搪瓷反应釜、山东搪玻璃反应釜等产品,参数说明详细,,订购价格有优惠 网站地图